प्रत्येक व्यक्ति अपने जीवन के दौरान ऐसे शरीरों का सामना करता है जो पदार्थ की तीन समग्र अवस्थाओं में से एक में होते हैं। अध्ययन के लिए एकत्रीकरण की सबसे सरल अवस्था गैस है। लेख में, हम एक आदर्श गैस की अवधारणा पर विचार करेंगे, सिस्टम की स्थिति का समीकरण देंगे, और निरपेक्ष तापमान के विवरण पर भी कुछ ध्यान देंगे।
पदार्थ की गैस अवस्था
प्रत्येक छात्र को इस बात का अच्छा अंदाजा होता है कि "गैस" शब्द सुनते ही वे किस स्थिति के बारे में बात कर रहे हैं। इस शब्द को एक शरीर के रूप में समझा जाता है जो इसे प्रदान की गई किसी भी मात्रा पर कब्जा करने में सक्षम है। यह अपने आकार को बनाए रखने में सक्षम नहीं है, क्योंकि यह मामूली बाहरी प्रभाव का भी विरोध नहीं कर सकता है। इसके अलावा, गैस मात्रा को बरकरार नहीं रखती है, जो इसे न केवल ठोस से, बल्कि तरल पदार्थों से भी अलग करती है।
तरल की तरह गैस भी एक तरल पदार्थ है। गैसों में ठोस पिंडों की गति की प्रक्रिया में, बाद वाले इस गति में बाधा डालते हैं। परिणामी बल को प्रतिरोध कहते हैं। इसका मूल्य निर्भर करता हैगैस में पिंड का वेग।
गैसों के प्रबल उदाहरण हैं हवा, घरों को गर्म करने और खाना पकाने के लिए उपयोग की जाने वाली प्राकृतिक गैस, विज्ञापन चमकने वाली ट्यूबों को भरने के लिए अक्रिय गैसों (Ne, Ar) का उपयोग किया जाता है या वेल्डिंग करते समय एक निष्क्रिय (गैर-आक्रामक, सुरक्षात्मक) वातावरण बनाने के लिए उपयोग किया जाता है।.
आदर्श गैस
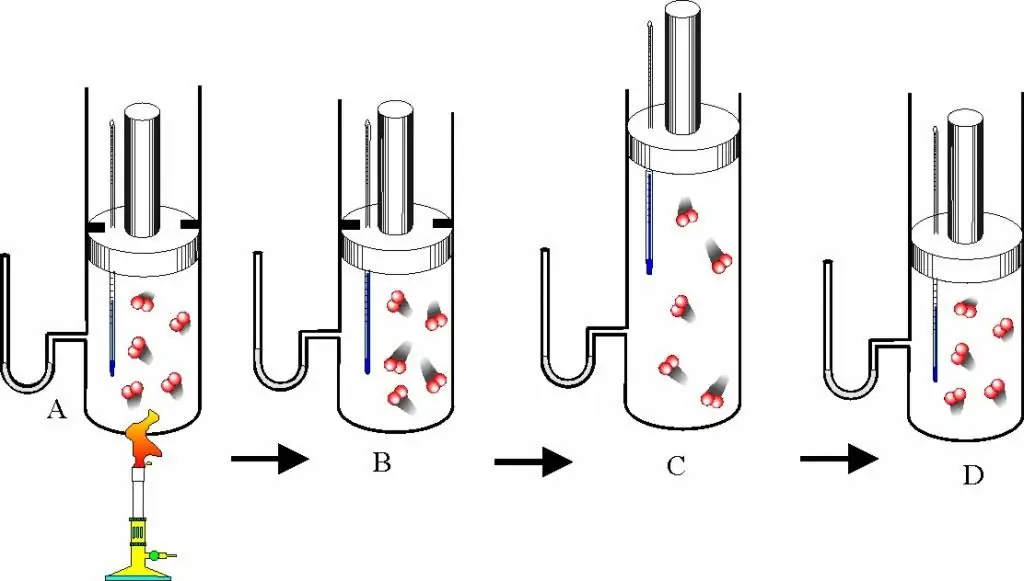
गैस कानूनों और राज्य के समीकरण के विवरण पर आगे बढ़ने से पहले, आपको इस प्रश्न को अच्छी तरह से समझना चाहिए कि एक आदर्श गैस क्या है। यह अवधारणा आणविक गतिज सिद्धांत (MKT) में पेश की गई है। एक आदर्श गैस कोई भी गैस है जो निम्नलिखित विशेषताओं को पूरा करती है:
- इसे बनाने वाले कण प्रत्यक्ष यांत्रिक टक्करों को छोड़कर एक दूसरे के साथ परस्पर क्रिया नहीं करते हैं।
- कणों के बर्तन की दीवारों से या आपस में टकराने के परिणामस्वरूप उनकी गतिज ऊर्जा और संवेग संरक्षित रहता है, अर्थात टक्कर पूर्णतया लोचदार मानी जाती है।
- कणों का कोई आयाम नहीं होता है, लेकिन उनका एक सीमित द्रव्यमान होता है, यानी वे भौतिक बिंदुओं के समान होते हैं।
स्वाभाविक है कि कोई भी गैस आदर्श नहीं बल्कि वास्तविक होती है। फिर भी, कई व्यावहारिक समस्याओं को हल करने के लिए, ये अनुमान काफी मान्य हैं और इनका उपयोग किया जा सकता है। एक सामान्य अनुभवजन्य नियम है जो कहता है: रासायनिक प्रकृति की परवाह किए बिना, यदि किसी गैस का तापमान कमरे के तापमान से ऊपर है और वायुमंडलीय या निम्न के क्रम का दबाव है, तो इसे उच्च सटीकता के साथ आदर्श माना जा सकता है और इसका वर्णन करने के लिए इस्तेमाल किया जा सकता है यह।राज्य के आदर्श गैस समीकरण का सूत्र।
क्लैपेरॉन-मेंडेलीव कानून
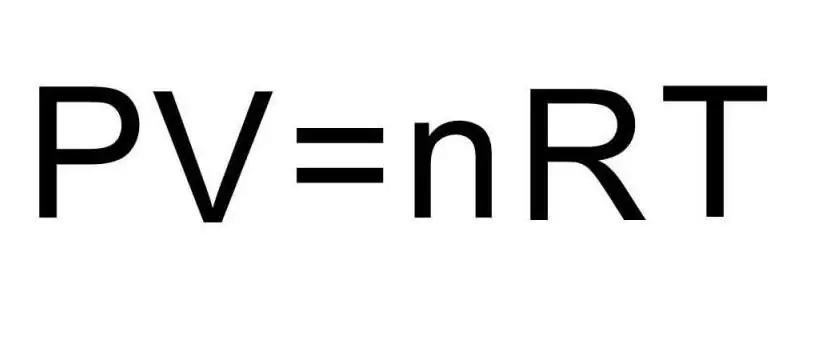
एक ही समुच्चय अवस्था के भीतर पदार्थ और प्रक्रियाओं की विभिन्न समुच्चय अवस्थाओं के बीच संक्रमण को थर्मोडायनामिक्स द्वारा नियंत्रित किया जाता है। दबाव, तापमान और आयतन तीन मात्राएँ हैं जो थर्मोडायनामिक प्रणाली की किसी भी स्थिति को विशिष्ट रूप से परिभाषित करती हैं। एक आदर्श गैस की अवस्था के समीकरण का सूत्र इन तीनों मात्राओं को एक समानता में जोड़ता है। आइए इस सूत्र को लिखें:
पीवी=एनआरटी
यहाँ P, V, T - दाब, आयतन, तापमान, क्रमशः। n का मान मोल में पदार्थ की मात्रा है, और प्रतीक R गैसों के सार्वभौमिक स्थिरांक को दर्शाता है। यह समानता दर्शाती है कि दबाव और आयतन का उत्पाद जितना अधिक होगा, पदार्थ की मात्रा और तापमान का उत्पाद उतना ही अधिक होना चाहिए।

गैस की अवस्था के समीकरण के सूत्र को क्लैपेरॉन-मेंडेलीव नियम कहते हैं। 1834 में, फ्रांसीसी वैज्ञानिक एमिल क्लैपेरॉन ने अपने पूर्ववर्तियों के प्रयोगात्मक परिणामों को संक्षेप में प्रस्तुत किया, इस समीकरण पर आए। हालांकि, क्लैपेरॉन ने कई स्थिरांक का उपयोग किया, जिसे बाद में मेंडेलीव ने एक के साथ बदल दिया - सार्वभौमिक गैस स्थिरांक R (8, 314 J / (molK))। इसलिए आधुनिक भौतिकी में इस समीकरण का नाम फ्रांसीसी और रूसी वैज्ञानिकों के नाम पर रखा गया है।

अन्य समीकरण प्रपत्र
ऊपर, हमने आम तौर पर स्वीकृत और में एक आदर्श गैस के लिए राज्य के मेंडेलीव-क्लैपेरॉन समीकरण को लिखा थासुविधाजनक रूप। हालांकि, ऊष्मप्रवैगिकी में समस्याओं में, अक्सर थोड़ा अलग रूप की आवश्यकता हो सकती है। तीन और सूत्र नीचे लिखे गए हैं, जो सीधे लिखित समीकरण से अनुसरण करते हैं:
पीवी=एनकेबीटी;
पीवी=एम/एमआरटी;
पी=आरटी/एम.
ये तीनों समीकरण एक आदर्श गैस के लिए भी सार्वत्रिक हैं, इनमें केवल द्रव्यमान m, दाढ़ द्रव्यमान M, घनत्व जैसी मात्राएँ और निकाय बनाने वाले कणों N की संख्या दिखाई देती है। प्रतीक kB यहां बोल्ट्जमान स्थिरांक को दर्शाता है (1, 3810-23J/K)।
बॉयल-मैरियट कानून
जब क्लैपेरॉन ने अपना समीकरण बनाया, तो वह गैस कानूनों पर आधारित था जिसे कई दशक पहले प्रयोगात्मक रूप से खोजा गया था। उनमें से एक बॉयल-मैरियोट कानून है। यह एक बंद प्रणाली में एक इज़ोटेर्मल प्रक्रिया को दर्शाता है, जिसके परिणामस्वरूप दबाव और आयतन जैसे मैक्रोस्कोपिक पैरामीटर बदल जाते हैं। यदि हम एक आदर्श गैस के लिए राज्य के समीकरण में T और n स्थिरांक रखते हैं, तो गैस कानून का रूप लेगा:
पी1वी1=पी2वी 2
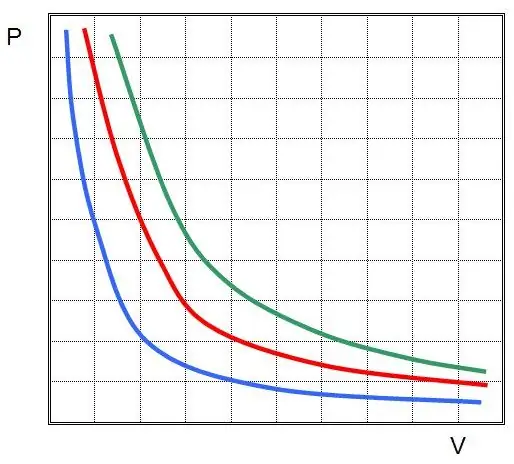
यह बॉयल-मैरियोट का नियम है, जो कहता है कि दबाव और आयतन के उत्पाद को एक मनमानी इज़ोटेर्मल प्रक्रिया के दौरान संरक्षित किया जाता है। इस मामले में, मान P और V स्वयं बदल जाते हैं।
यदि आप P(V) या V(P) प्लॉट करते हैं, तो समताप रेखा अतिपरवलय होगी।
चार्ल्स और गे-लुसाक के नियम
ये कानून गणितीय रूप से समदाब रेखीय और समद्विबाहु का वर्णन करते हैंप्रक्रियाएं, अर्थात्, गैस प्रणाली की अवस्थाओं के बीच ऐसे संक्रमण, जिसमें क्रमशः दबाव और आयतन संरक्षित होते हैं। चार्ल्स के नियम को गणितीय रूप से इस प्रकार लिखा जा सकता है:
V/T=const जब n, P=const.
गे-लुसाक का नियम इस प्रकार लिखा गया है:
P/T=const जब n, V=const.
यदि दोनों समानताएं एक ग्राफ के रूप में प्रस्तुत की जाती हैं, तो हमें सीधी रेखाएं मिलेंगी जो किसी कोण पर x-अक्ष पर झुकी होती हैं। इस प्रकार का ग्राफ स्थिर दबाव पर आयतन और तापमान के बीच और स्थिर आयतन पर दबाव और तापमान के बीच प्रत्यक्ष आनुपातिकता को दर्शाता है।
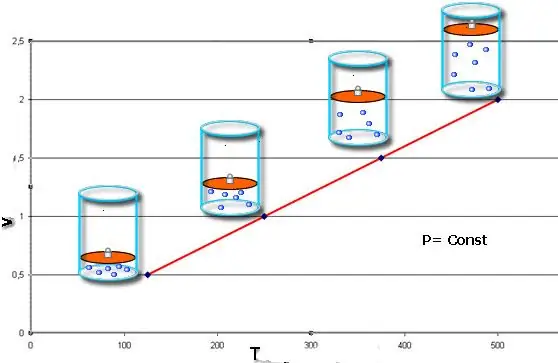
ध्यान दें कि तीनों माने जाने वाले गैस कानून गैस की रासायनिक संरचना, साथ ही इसके पदार्थ की मात्रा में परिवर्तन को ध्यान में नहीं रखते हैं।
पूर्ण तापमान
रोजमर्रा की जिंदगी में, हम सेल्सियस तापमान पैमाने का उपयोग करने के आदी हैं, क्योंकि यह हमारे आसपास की प्रक्रियाओं का वर्णन करने के लिए सुविधाजनक है। तो, पानी 100 oC पर उबलता है और 0 oC पर जम जाता है। भौतिकी में, यह पैमाना असुविधाजनक हो जाता है, इसलिए तथाकथित निरपेक्ष तापमान पैमाने का उपयोग किया जाता है, जिसे 19 वीं शताब्दी के मध्य में लॉर्ड केल्विन द्वारा पेश किया गया था। इस पैमाने के अनुसार तापमान को केल्विन (K) में मापा जाता है।
ऐसा माना जाता है कि -273, 15 oC के तापमान पर परमाणुओं और अणुओं के ऊष्मीय कंपन नहीं होते हैं, उनकी आगे की गति पूरी तरह से रुक जाती है। डिग्री सेल्सियस में यह तापमान केल्विन (0 K) में परम शून्य से मेल खाता है। इस परिभाषा सेनिरपेक्ष तापमान का भौतिक अर्थ इस प्रकार है: यह उन कणों की गतिज ऊर्जा का माप है जो पदार्थ बनाते हैं, उदाहरण के लिए, परमाणु या अणु।
निरपेक्ष तापमान के उपरोक्त भौतिक अर्थ के अलावा, इस मात्रा को समझने के अन्य तरीके भी हैं। उनमें से एक चार्ल्स का उल्लिखित गैस नियम है। आइए इसे निम्नलिखित रूप में लिखें:
वी1/टी1=वी2/टी 2=>
वी1/वी2=टी1/टी 2.
अंतिम समानता कहती है कि सिस्टम में पदार्थ की एक निश्चित मात्रा (उदाहरण के लिए, 1 mol) और एक निश्चित दबाव (उदाहरण के लिए, 1 Pa) पर, गैस की मात्रा विशिष्ट रूप से निरपेक्ष तापमान को निर्धारित करती है। दूसरे शब्दों में, इन परिस्थितियों में गैस की मात्रा में वृद्धि तापमान में वृद्धि के कारण ही संभव है, और मात्रा में कमी टी के मूल्य में कमी का संकेत देती है।
याद रखें कि, सेल्सियस तापमान के विपरीत, पूर्ण तापमान नकारात्मक नहीं हो सकता।
आवोगाद्रो सिद्धांत और गैस मिश्रण
उपरोक्त गैस कानूनों के अलावा, एक आदर्श गैस के लिए राज्य का समीकरण भी 19 वीं शताब्दी की शुरुआत में एमेडियो अवोगाद्रो द्वारा खोजे गए सिद्धांत की ओर ले जाता है, जो उनका अंतिम नाम है। यह सिद्धांत स्थापित करता है कि स्थिर दबाव और तापमान पर किसी भी गैस की मात्रा प्रणाली में पदार्थ की मात्रा से निर्धारित होती है। संबंधित सूत्र इस तरह दिखता है:
n/V=const जब P, T=const.
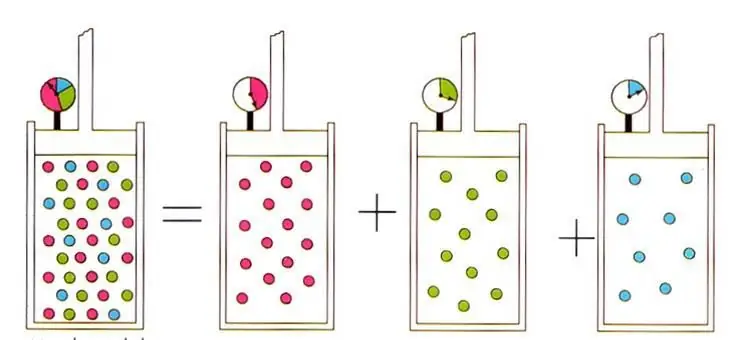
लिखित अभिव्यक्ति आदर्श गैस भौतिकी में जाने-माने गैस मिश्रण के लिए डाल्टन के नियम की ओर ले जाती है। यहकानून कहता है कि मिश्रण में गैस का आंशिक दबाव विशिष्ट रूप से उसके परमाणु अंश द्वारा निर्धारित किया जाता है।
समस्या समाधान का उदाहरण
आदर्श गैस युक्त कठोर दीवारों वाले बंद बर्तन में, गर्म करने के परिणामस्वरूप, दबाव 3 गुना बढ़ जाता है। सिस्टम का अंतिम तापमान निर्धारित करना आवश्यक है यदि इसका प्रारंभिक मान 25 oC.
था।
सबसे पहले, तापमान को डिग्री सेल्सियस से केल्विन में बदलते हैं, हमारे पास:
टी=25 + 273, 15=298, 15 के.
चूंकि बर्तन की दीवारें कठोर हैं, इसलिए हीटिंग प्रक्रिया को आइसोकोरिक माना जा सकता है। इस मामले के लिए, हम गे-लुसाक कानून लागू करते हैं, हमारे पास:
पी1/टी1=पी2/टी 2=>
टी2=पी2/पी1टी 1.
इस प्रकार, अंतिम तापमान दबाव अनुपात और प्रारंभिक तापमान के गुणनफल से निर्धारित होता है। डेटा को समानता में प्रतिस्थापित करने पर, हमें उत्तर मिलता है: T2=894.45 K. यह तापमान 621.3 oC.
से मेल खाता है।






